Trong hành trình tìm kiếm hy vọng cho người bệnh ung thư, có những loại thuốc không chỉ mang lại thêm thời gian — mà còn mở ra một cách tiếp cận hoàn toàn mới. Keytruda (tên hoạt chất Pembrolizumab) là một trong số đó.
Nếu hóa trị được ví như “búa tạ” tấn công trực tiếp tế bào ung thư — dù đôi khi làm tổn thương cả tế bào khỏe mạnh — thì Keytruda lại chọn cách thông minh hơn: đánh thức chính hệ miễn dịch của cơ thể để nhận diện và tiêu diệt tế bào ung thư.
Thuốc này là một kháng thể đơn dòng – dạng protein sinh học được “nhân hóa” trong phòng thí nghiệm, thuộc nhóm liệu pháp miễn dịch (immunotherapy). Cơ chế hoạt động của nó không phải tiêu diệt khối u bằng hóa chất, mà là gỡ bỏ “tấm khiên ngụy trang” mà tế bào ung thư dùng để trốn tránh hệ miễn dịch.
Công nghệ đằng sau Pembrolizumab được phát triển bởi hãng dược phẩm Merck Sharp & Dohme (MSD) – một trong những tập đoàn tiên phong trong lĩnh vực miễn dịch ung thư. Trên hệ thống phân loại thuốc quốc tế (ATC), Keytruda được xếp vào nhóm L01XC18 – Thuốc chống ung thư, kháng thể đơn dòng, khẳng định vị thế của nó như một trụ cột của kỷ nguyên điều trị mới.
Tại Việt Nam, Keytruda không chỉ là một tên thuốc – nó là biểu tượng của sự thay đổi: từ điều trị bằng thuốc tấn công sang điều trị bằng trí tuệ sinh học của cơ thể. Tuy nhiên, hành trình để bệnh nhân tiếp cận với liệu pháp tiên tiến này vẫn còn nhiều rào cản, từ thủ tục đăng ký, giá thuốc, cho đến bảo hiểm và chính sách hỗ trợ.
Tổng quan về Pembrolizumab (Keytruda) – Một Trụ cột của Liệu pháp Miễn dịch Ung thư
Pembrolizumab, với tên thương mại phổ biến toàn cầu và tại Việt Nam là Keytruda, là một liệu pháp sinh học tiên tiến, đánh dấu một cuộc cách mạng trong điều trị ung thư. Đây không phải là hóa trị truyền thống tác động lên các tế bào phân chia nhanh, mà là một kháng thể đơn dòng nhân hóa (humanized monoclonal antibody) , thuộc nhóm liệu pháp miễn dịch (immunotherapy).
Về mặt dược lý, Pembrolizumab được phân loại trong Hệ thống phân loại Giải phẫu Trị liệu Hóa học (ATC) với mã L01XC18, thuộc nhóm “Thuốc chống ung thư” và cụ thể hơn là “Kháng thể đơn dòng”. Thuốc được nghiên cứu và phát triển bởi tập đoàn dược phẩm Merck, Sharp & Dohme (MSD), đơn vị cũng đồng thời tài trợ cho các chương trình hỗ trợ bệnh nhân lớn tại Việt Nam.
Vai trò của Pembrolizumab mang tính đột phá: thay vì trực tiếp tiêu diệt tế bào ung thư, nó hoạt động bằng cách kích hoạt và “vũ khí hóa” chính hệ thống miễn dịch của bệnh nhân để nhận diện và tiêu diệt các tế bào ác tính. Sự ra đời của nó đã làm thay đổi căn bản phác đồ điều trị cho nhiều loại ung thư, mang lại hy vọng cho những bệnh nhân ở giai đoạn tiến triển hoặc di căn.

Cơ chế Hoạt động: “Tháo phanh” cho Hệ thống Miễn dịch
Để hiểu cơ chế của Pembrolizumab, trước tiên cần hiểu cách các tế bào ung thư trốn tránh hệ thống miễn dịch.
Giải thích về Điểm kiểm soát Miễn dịch và Sự trốn tránh của Khối u
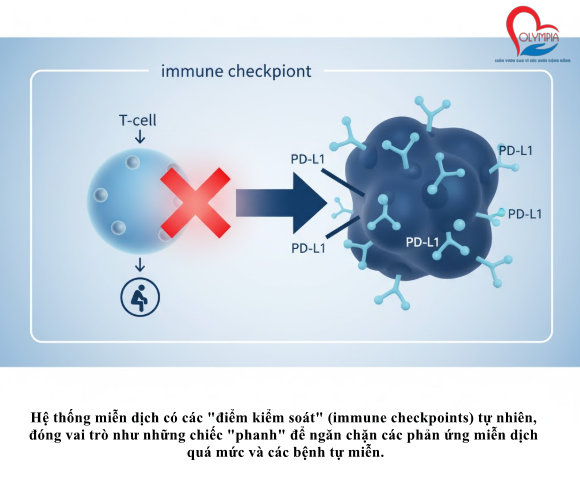
Hệ thống miễn dịch có các “điểm kiểm soát” (immune checkpoints) tự nhiên, đóng vai trò như những chiếc “phanh” để ngăn chặn các phản ứng miễn dịch quá mức và các bệnh tự miễn. Một trong những điểm kiểm soát quan trọng nhất là protein $PD-1$ (Programmed Cell Death Protein 1), được biểu hiện trên bề mặt các tế bào miễn dịch (như tế bào T).
Nhiều tế bào ung thư đã “học” cách khai thác cơ chế này. Chúng biểu hiện các phối tử (ligands) trên bề mặt của chúng, gọi là $PD-L1$ và $PD-L2$. Khi $PD-L1$ hoặc $PD-L2$ trên tế bào ung thư liên kết với $PD-1$ trên tế bào T, nó sẽ gửi một tín hiệu “dừng” hoặc “tắt” (negative signals) đến tế bào T. Điều này làm cho tế bào T trở nên kiệt sức (exhausted effector T-cell phenotype) và mất khả năng tấn công khối u. Đây là một trong những cơ chế trốn tránh miễn dịch (immune evasion) tinh vi và hiệu quả nhất của ung thư.
Cơ chế Phân tử của Pembrolizumab
Pembrolizumab là một kháng thể đơn dòng được thiết kế đặc biệt để kháng $PD-1$ (anti-$PD-1$ antibody).
Cơ chế của nó diễn ra như sau: Pembrolizumab liên kết có chọn lọc và chặn protein $PD-1$ trên các tế bào T.1 Bằng cách chiếm lấy $PD-1$, Pembrolizumab ngăn chặn một cách vật lý sự tương tác giữa $PD-1$ (trên tế bào T) và $PD-L1$/$PD-L2$ (trên tế bào ung thư).
Hành động này đã “tháo bỏ” chiếc phanh miễn dịch. Tín hiệu “tắt” bị chặn lại. Kết quả là, các tế bào T được “tái kích hoạt”, phục hồi khả năng nhận diện khối u và thực hiện chức năng tiêu diệt tế bào ung thư một cách hiệu quả.
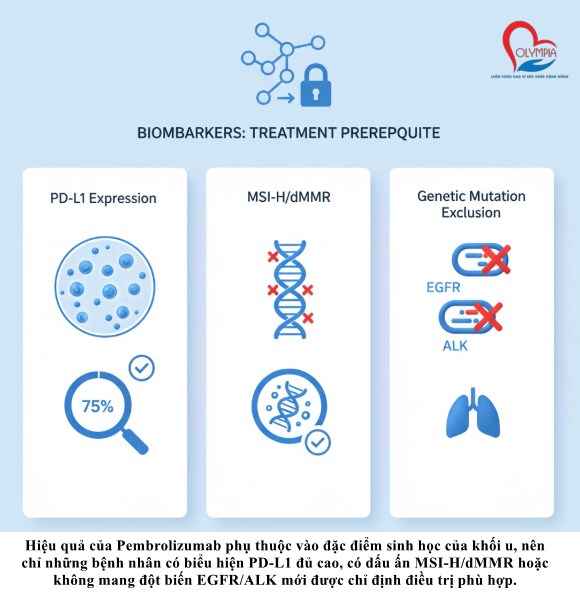
Dấu ấn Sinh học (Biomarkers): Điều kiện Tiên quyết để Điều trị
Hiệu quả của Pembrolizumab không đồng đều ở tất cả các bệnh nhân. Do đó, việc điều trị đòi hỏi phải có các xét nghiệm dấu ấn sinh học tiên quyết để lựa chọn bệnh nhân phù hợp.
- Biểu hiện $PD-L1$: Đối với nhiều loại ung thư (như ung thư phổi không tế bào nhỏ, ung thư đầu và cổ), bệnh nhân phải được xét nghiệm mức độ biểu hiện $PD-L1$ trên khối u hoặc các tế bào miễn dịch xung quanh. Kết quả này được báo cáo dưới dạng TPS (Tumor Proportion Score) hoặc CPS (Combined Positive Score). Ví dụ, chỉ định điều trị NSCLC hàng đầu yêu cầu TPS $\geq$ 1% , trong khi chỉ định HNSCC yêu cầu CPS $\geq$ 1.
- MSI-H/dMMR: Một dấu ấn sinh học quan trọng khác là MSI-H (Microsatellite Instability-High), tức là Mất ổn định Vi vệ tinh Mức độ cao, hoặc dMMR (Mismatch Repair Deficient), tức là Khiếm khuyết Sửa chữa Bắt cặp Sai. Các khối u có đặc điểm này thường có gánh nặng đột biến (high gene mutation burdens) cao, tạo ra nhiều “kháng nguyên mới” (neo-antigens) hơn, khiến chúng trở thành mục tiêu rõ ràng hơn cho hệ miễn dịch được tái kích hoạt. Chỉ định MSI-H/dMMR là một bước ngoặt, vì đây là điều trị “bất khả tri về khối u” (tumor-agnostic), nghĩa là nó dựa trên đặc điểm di truyền của khối u chứ không phải vị trí giải phẫu của nó.
- Loại trừ Đột biến Gen: Đối với ung thư phổi không tế bào nhỏ (NSCLC), việc sử dụng Pembrolizumab đơn trị liệu hàng đầu cũng yêu cầu bệnh nhân không có các đột biến gen $EGFR$ hoặc $ALK$.
Những yêu cầu về dấu ấn sinh học này hàm ý rằng, để tiếp cận điều trị bằng Pembrolizumab tại Việt Nam, bệnh nhân phải vượt qua hai rào cản: rào cản tài chính (sẽ thảo luận ở Phần VII) và rào cản về cơ sở hạ tầng chẩn đoán. Các bệnh viện (trong số 49 cơ sở tham gia chương trình hỗ trợ) phải có năng lực thực hiện các xét nghiệm hóa mô miễn dịch (để đo TPS/CPS) và xét nghiệm di truyền phân tử (để xác định MSI-H/dMMR) theo các tiêu chuẩn nghiêm ngặt.
Phổ Chỉ định Lâm sàng Rộng rãi của Pembrolizumab
Pembrolizumab đã được phê duyệt cho một danh sách dài các chỉ định ung thư trên toàn thế giới (bởi FDA, EMA) và được áp dụng rộng rãi tại Việt Nam. Danh sách các bệnh được chấp thuận trong chương trình hỗ trợ chính thức tại Việt Nam là bằng chứng thực tế nhất về phạm vi điều trị của thuốc.
Các chỉ định chính bao gồm:
- Ung thư Phổi Không Tế bào Nhỏ (NSCLC):
- Điều trị hàng đầu (first-line) đơn trị liệu: Cho bệnh nhân Giai đoạn III không thể phẫu thuật hoặc hóa xạ trị, hoặc Giai đoạn IV (di căn), có biểu hiện $PD-L1$ (TPS $\geq$ 1%) và không có đột biến $EGFR$/$ALK$.
- Điều trị hàng đầu kết hợp hóa trị: Cho bệnh nhân NSCLC di căn, bất kể mức độ $PD-L1$.
- Điều trị bổ trợ (Adjuvant): Sau phẫu thuật và hóa trị, cho bệnh nhân NSCLC Giai đoạn IB (khối u $\geq$ 4 cm), Giai đoạn II, hoặc Giai đoạn IIIA, để giảm nguy cơ tái phát.
- Điều trị tân bổ trợ (Neoadjuvant): Kết hợp với hóa trị trước phẫu thuật, sau đó tiếp tục đơn trị liệu sau phẫu thuật cho NSCLC có thể cắt bỏ (T$\geq$4 cm hoặc N+).
- U hắc tố (Melanoma):
- Điều trị u hắc tố tiến triển (di căn hoặc không thể cắt bỏ).
- Điều trị bổ trợ cho bệnh nhân Giai đoạn IIB, IIC, hoặc III (người lớn và trẻ em từ 12 tuổi) sau khi đã phẫu thuật cắt bỏ hoàn toàn khối u và hạch, để ngăn ngừa tái phát. Các nghiên cứu cho thấy Pembrolizumab vượt trội hơn Ipilimumab (một chất ức chế $CTLA-4$ khác) trong điều trị u hắc tố Giai đoạn III/IV không thể cắt bỏ.
- Ung thư Đầu và Cổ (HNSCC):
- Điều trị hàng đầu đơn trị liệu: Cho bệnh nhân di căn hoặc tái phát không thể cắt bỏ, có biểu hiện $PD-L1$ (CPS $\geq$ 1).
- Điều trị hàng hai (second-line): Cho bệnh nhân tái phát hoặc di căn có bệnh tiến triển trong hoặc sau khi hóa trị chứa platinum.
- Ung thư Biểu mô Đường tiết niệu (Urothelial Carcinoma) (Ung thư bàng quang):
- Điều trị ung thư bàng quang không xâm lấn cơ (NMIBC) nguy cơ cao, không đáp ứng với liệu pháp BCG, có carcinoma in situ (CIS), ở những bệnh nhân không đủ điều kiện hoặc đã chọn không phẫu thuật cắt bỏ bàng quang.
- Các Khối u Rắn có MSI-H/dMMR:
- Chỉ định “bất khả tri về khối u” cho bệnh nhân người lớn và trẻ em có các khối u rắn không thể cắt bỏ hoặc di căn, có tình trạng MSI-H hoặc dMMR, đã tiến triển sau các phương pháp điều trị trước đó và không còn lựa chọn điều trị thay thế nào.
- Các Chỉ định khác được phê duyệt và hỗ trợ tại Việt Nam :
- U lympho Hodgkin kinh điển (cHL)
- Ung thư dạ dày
- Ung thư cổ tử cung
- Ung thư biểu mô tế bào gan (HCC)
- Ung thư đại-trực tràng (có tình trạng MSI-H/dMMR)
- U lympho tế bào B lớn trung thất nguyên phát (PMBCL)
- Ung thư thực quản
- Ung thư vú bộ ba âm tính
Phạm vi chỉ định rộng rãi này, bao gồm cả các loại ung thư hiếm (PMBCL) và các chỉ định dựa trên di truyền (MSI-H), cho thấy sự đồng bộ nhanh chóng của các phác đồ điều trị ung thư tiên tiến tại Việt Nam với các tiêu chuẩn toàn cầu.
Hướng dẫn Quản lý và Liều dùng Tiêu chuẩn
Việc sử dụng Pembrolizumab đòi hỏi tuân thủ nghiêm ngặt các hướng dẫn về đường dùng, liều lượng và thời gian.
- Đường dùng: Keytruda được dùng nghiêm ngặt qua đường truyền tĩnh mạch (intravenous infusion).
- Cảnh báo Quản lý: Thuốc không được dùng dưới dạng tiêm tĩnh mạch nhanh hoặc tiêm bolus tĩnh mạch (tiêm một liều lượng lớn và nhanh).
- Thời gian Truyền: Mỗi lần truyền thường kéo dài trong khoảng 30 phút.
- Dạng bào chế tại Việt Nam: Thông tin đăng ký chính thức cho thấy dạng bào chế có sẵn là lọ dung dịch đậm đặc để pha tiêm truyền, hàm lượng 100mg/4ml.
Các Phác đồ Liều dùng Phổ biến
Các phác đồ liều dùng sau đây được áp dụng phổ biến, tùy thuộc vào chỉ định và đối tượng bệnh nhân:
- Phác đồ 3 tuần: 200 mg truyền tĩnh mạch mỗi 3 tuần. Đây là phác đồ tiêu chuẩn cho hầu hết các chỉ định ở người lớn, bao gồm NSCLC, u lympho Hodgkin kinh điển, ung thư biểu mô đường tiết niệu, ung thư đầu và cổ, v.v..
- Phác đồ 6 tuần (Người lớn): 400 mg truyền tĩnh mạch mỗi 6 tuần. Đây là một lựa chọn thay thế, giúp giảm số lần bệnh nhân phải đến bệnh viện, mang lại sự thuận tiện hơn.
- Liều dựa trên Cân nặng: Một số chỉ định (ví dụ: u hắc tố ác tính, NSCLC đã điều trị trước đây) và đặc biệt là ở bệnh nhi (dưới 18 tuổi) sử dụng liều 2 mg/kg truyền tĩnh mạch mỗi 3 tuần.
Một phân tích quan trọng khi kết hợp thông tin liều dùng và dạng bào chế tại Việt Nam là về mặt chi phí và hỗ trợ. Với dạng bào chế là 100mg/4ml , một bệnh nhân người lớn dùng liều tiêu chuẩn 200mg sẽ cần 2 lọ cho mỗi lần truyền, và bệnh nhân dùng liều 400mg sẽ cần 4 lọ.
Sự tính toán này làm sáng tỏ cơ cấu của “Chương trình Hỗ trợ Thuốc Keytruda” (thảo luận ở Phần VII). Ví dụ, Mức hỗ trợ 1 cho liều 200mg là “người bệnh tự chi trả 01 lọ thuốc và được nhận 01 lọ thuốc miễn phí”.4 Điều này hoàn toàn khớp với nhu cầu 2 lọ thuốc, về cơ bản là một chương trình “mua 1 tặng 1”, tương đương với việc giảm 50% chi phí thuốc cho bệnh nhân. Tương tự, Mức hỗ trợ 1 cho liều 400mg (cần 4 lọ) là “tự chi trả 02 lọ thuốc và được nhận 02 lọ thuốc miễn phí” , cũng là một chương trình “mua 2 tặng 2”, duy trì mức hỗ trợ 50%.
Hồ sơ An toàn Toàn diện và Quản lý Tác dụng phụ
Trọng tâm của liệu pháp miễn dịch nằm ở một nghịch lý: cơ chế “tháo phanh” miễn dịch để tiêu diệt ung thư cũng chính là nguồn gốc của các tác dụng phụ độc đáo và nghiêm trọng. Khi hệ thống miễn dịch được kích hoạt, nó không chỉ tấn công các tế bào ung thư mà còn có thể tấn công các cơ quan và mô khỏe mạnh, gây ra các phản ứng viêm.
Những tác dụng phụ này được gọi là Tác dụng phụ liên quan đến Miễn dịch (irAEs – Immune-Related Adverse Events). Chúng có thể trở nên nghiêm trọng, đe dọa tính mạng và có thể xảy ra bất cứ lúc nào trong quá trình điều trị, hoặc thậm chí vài tháng sau khi kết thúc điều trị.
Tác dụng phụ Nghiêm trọng (irAEs) – Cần Can thiệp Y tế Ngay lập tức
Bệnh nhân và người nhà phải được giáo dục kỹ lưỡng để nhận biết và báo cáo ngay lập tức cho bác sĩ nếu xuất hiện bất kỳ dấu hiệu hoặc triệu chứng nào sau đây:
- Vấn đề về Phổi (Viêm phổi – Pneumonitis): Biểu hiện qua ho (mới hoặc nặng hơn), đau ngực, hoặc khó thở.
- Vấn đề về Đường ruột (Viêm đại tràng – Colitis): Tiêu chảy (phân lỏng, đi tiêu thường xuyên hơn bình thường), phân có màu đen, hắc ín, hoặc có máu/chất nhầy, đau bụng dữ dội.
- Vấn đề về Gan (Viêm gan – Hepatitis): Vàng da hoặc vàng lòng trắng mắt, buồn nôn hoặc nôn mửa nghiêm trọng, đau ở phía bên phải vùng bụng, nước tiểu sẫm màu (như màu trà), dễ chảy máu hoặc bầm tím hơn bình thường.8
- Vấn đề về Nội tiết (Endocrinopathies): Viêm các tuyến hormone (tuyến giáp, tuyến yên, tuyến thượng thận). Các triệu chứng thường không đặc hiệu và đa dạng, bao gồm: nhức đầu liên tục hoặc bất thường, nhạy cảm với ánh sáng, các vấn đề về mắt, mệt mỏi cùng cực, tăng hoặc giảm cân không rõ nguyên nhân, cảm thấy đói hoặc khát nhiều hơn bình thường, rụng tóc, cảm thấy lạnh, táo bón, chóng mặt hoặc ngất xỉu, thay đổi tâm trạng hoặc hành vi (cáu kỉnh, hay quên). Có thể gây ra bệnh tiểu đường loại 1.
- Vấn đề về Thận (Viêm thận – Nephritis): Giảm lượng nước tiểu, có máu trong nước tiểu, sưng mắt cá chân, chán ăn.
- Vấn đề về Da: Phát ban nghiêm trọng, da bị phồng rộp hoặc bong tróc, vết loét hoặc vết loét đau đớn trong miệng, mũi, họng hoặc vùng sinh dục, sốt hoặc các triệu chứng giống cúm.
- Các vấn đề về Cơ quan Khác:
- Thần kinh: Lú lẫn, buồn ngủ, các vấn đề về trí nhớ, cứng cổ, các vấn đề về thăng bằng, tê hoặc ngứa ran ở cánh tay hoặc chân (có thể là hội chứng Guillain-Barré).
- Tim: Viêm cơ tim (đau ngực, nhịp tim không đều, khó thở).3
- Mắt: Nhìn đôi, nhìn mờ, nhạy cảm với ánh sáng, đau mắt, thay đổi thị lực.8
- Phản ứng Truyền dịch: Các triệu chứng xảy ra trong hoặc ngay sau khi truyền thuốc, bao gồm ớn lạnh hoặc run, ngứa hoặc phát ban, đỏ bừng, khó thở, chóng mặt, sốt.
- Biến chứng Cấy ghép: Có thể gây thải ghép cơ quan hoặc mô được cấy ghép.8 Đặc biệt, có nguy cơ cao gây ra bệnh mảnh ghép chống lại vật chủ (GVHD) ở những người đã hoặc dự định cấy ghép tủy xương (tế bào gốc) dị thân.8
Tác dụng phụ Phổ biến (Thường gặp và Ít nghiêm trọng hơn)
Ngoài các irAEs nghiêm trọng, bệnh nhân cũng có thể gặp các tác dụng phụ phổ biến và nhẹ hơn, bao gồm:
- Cảm thấy mệt mỏi (fatigue) 3
- Đau (đau cơ, đau xương khớp, đau bụng) 3
- Phát ban da, ngứa 3
- Tiêu chảy (mức độ nhẹ) 8
- Sốt 3
- Ho 3
- Giảm cảm giác ngon miệng 3
- Buồn nôn 3
- Táo bón 8
- Nồng độ hormone tuyến giáp thấp (suy giáp) 3
Bảng dưới đây tóm tắt sự khác biệt quan trọng mà bệnh nhân cần lưu ý.
Bảng 1: Phân biệt Tác dụng phụ Phổ biến và Tác dụng phụ Nghiêm trọng (irAEs) của Pembrolizumab
|
Hệ cơ quan |
Tác dụng phụ Phổ biến (Có thể quản lý) |
Tác dụng phụ Nghiêm trọng (irAEs) – BÁO BÁC SĨ NGAY |
|
Phổi |
Ho nhẹ |
Ho nặng hơn, đau ngực, khó thở (kể cả khi nghỉ ngơi) |
|
Đường ruột |
Buồn nôn, táo bón, tiêu chảy nhẹ |
Tiêu chảy nặng (nhiều lần/ngày), phân có máu hoặc chất nhầy, đau bụng dữ dội |
|
Gan |
(Thường không có triệu chứng) |
Vàng da, vàng mắt, nước tiểu sẫm màu, đau bụng trên bên phải, buồn nôn/nôn mửa |
|
Da |
Phát ban nhẹ, ngứa |
Phát ban nặng, phồng rộp, bong tróc da, loét đau ở miệng, mũi, vùng sinh dục |
|
Nội tiết |
Mệt mỏi (có thể liên quan đến suy giáp) |
Mệt mỏi cùng cực, nhức đầu liên tục, thay đổi cân nặng đột ngột, chóng mặt, ngất xỉu |
|
Toàn thân |
Mệt mỏi, sốt nhẹ, đau cơ khớp |
Sốt cao, ớn lạnh (có thể là phản ứng truyền dịch), mệt mỏi đến mức không thể sinh hoạt |
Chống chỉ định và Thận trọng Đặc biệt
- Chống chỉ định: Chống chỉ định tuyệt đối ở những bệnh nhân có tiền sử quá mẫn nghiêm trọng với hoạt chất Pembrolizumab hoặc bất kỳ thành phần tá dược nào của thuốc.
- Mang thai và Cho con bú:
- Không sử dụng cho phụ nữ có thai. Pembrolizumab có thể gây hại nghiêm trọng cho thai nhi.
- Phụ nữ có khả năng mang thai bắt buộc phải sử dụng các biện pháp tránh thai hiệu quả trong suốt quá trình điều trị VÀ trong ít nhất 4 tháng sau liều thuốc cuối cùng.
- Không cho con bú trong khi điều trị và trong 4 tháng sau liều cuối cùng, do chưa biết thuốc có đi vào sữa mẹ hay không.
Hồ sơ an toàn phức tạp này lý giải tại sao việc điều trị bằng Pembrolizumab tại Việt Nam được giới hạn trong các cơ sở y tế chuyên khoa (như 49 bệnh viện trong chương trình hỗ trợ), nơi có đội ngũ y tế được đào tạo để nhận biết sớm và xử lý kịp thời các độc tính miễn dịch này.4
Tình trạng Pháp lý và Đăng ký của Pembrolizumab tại Việt Nam
Pembrolizumab (Keytruda) đã được Cục Quản lý Dược – Bộ Y tế Việt Nam xem xét và cấp phép lưu hành chính thức, đảm bảo nguồn thuốc được nhập khẩu chính ngạch và kiểm soát chất lượng.
Thông tin nhận dạng pháp lý chính thức của thuốc tại Việt Nam như sau :
- Tên thương mại: Keytruda
- Hoạt chất: Pembrolizumab
- Dạng bào chế và Hàm lượng: Dung dịch đậm đặc để pha tiêm truyền, 100mg/4ml
- Số Đăng Ký (SĐK): QLSP-H02-1073-17
- Mã ATC: L01XC18
- Nhóm dược lý: Thuốc chống ung thư, kháng thể đơn dòng
Việc có Số Đăng Ký (SĐK) chính thức QLSP-H02-1073-17 là nền tảng pháp lý cho mọi hoạt động liên quan đến thuốc tại Việt Nam. Nó đảm bảo bệnh nhân được sử dụng “thuốc chuẩn” , và quan trọng hơn, cho phép Bộ Y tế ban hành các quyết định (như Quyết định số 2205/QĐ-BYT) để phê duyệt các chương trình hỗ trợ bệnh nhân quy mô lớn, hợp pháp.
Khả năng Tiếp cận tại Việt Nam: Chương trình Hỗ trợ Thuốc Keytruda (Giai đoạn 2024-2026)
Mặc dù có hiệu quả vượt trội, chi phí cho các liệu pháp miễn dịch như Pembrolizumab là một rào cản tài chính khổng lồ. Để giải quyết vấn đề này, một “hệ sinh thái” hỗ trợ đa bên đã được thiết lập tại Việt Nam.
Tổng quan Chương trình và các Bên liên quan
Chương trình hỗ trợ thuốc Keytruda (Pembrolizumab) giai đoạn 2024 – 2026 được triển khai trên toàn quốc.
- Thời gian: Chương trình diễn ra từ ngày 01/01/2024 đến 31/12/2026.
- Thời hạn Đăng ký: Thời gian tiếp nhận người bệnh mới đăng ký tham gia là từ 01/01/2024 đến 31/12/2025.
- Các bên Liên quan : Đây là một chương trình hợp tác công-tư phức tạp, bao gồm:
- Cơ quan Quản lý: Bộ Y tế (phê duyệt theo Quyết định 2205/QĐ-BYT).
- Nhà tài trợ: MSD (hãng sản xuất, tài trợ thuốc và tài chính).
- Đơn vị Điều phối: Quỹ Hỗ trợ Bệnh nhân Ung thư – Ngày mai tươi sáng.
- Đơn vị Phân phối: Công ty Phytopharma.
- Đơn vị Thẩm định: Công ty Cổ phần EasyGop (bên thứ ba độc lập, đánh giá khả năng chi trả).
- Đơn vị Điều trị: 49 bệnh viện điều trị ung thư trên toàn quốc.
Điều kiện Tham gia và Cấu trúc Hỗ trợ
- Điều kiện :
- Bệnh nhân là công dân Việt Nam.
- Được chẩn đoán mắc một trong các bệnh thuộc chỉ định dùng thuốc Keytruda đã được Bộ Y tế phê duyệt (xem danh sách chi tiết ở Phần III).
- Quy trình Đánh giá (Người lớn) : Bệnh nhân người lớn sẽ được Công ty EasyGop (bên thứ ba độc lập) đánh giá khả năng chi trả dựa trên bộ công cụ MBAT (Means-based Assessment Tool). Việc này nhằm phân bổ hỗ trợ một cách công bằng, ưu tiên hỗ trợ nhiều hơn cho những bệnh nhân có hoàn cảnh kinh tế khó khăn hơn.
- Mặc định: Trường hợp bệnh nhân không tham gia hoặc chưa tham gia đánh giá khả năng chi trả, bệnh nhân sẽ tự động được nhận Mức hỗ trợ 1.
Cấu trúc 3 Mức Hỗ trợ (Người lớn)
Chương trình chia thành 3 mức hỗ trợ dựa trên kết quả đánh giá của EasyGop.
Bảng 2: Cấu trúc Chương trình Hỗ trợ Bệnh nhân Keytruda (2024-2026) cho Người lớn
|
Mức hỗ trợ |
Điều kiện |
Cơ chế Hỗ trợ (Liều 200mg/3 tuần) |
Cơ chế Hỗ trợ (Liều 400mg/6 tuần) |
|
Mức 1 |
Mặc định (không cần đánh giá) hoặc kết quả đánh giá |
Người bệnh tự chi trả 01 lọ và được nhận 01 lọ miễn phí trong mỗi chu kỳ. |
Người bệnh tự chi trả 02 lọ và được nhận 02 lọ miễn phí trong mỗi chu kỳ. |
|
Mức 2 |
Kết quả đánh giá |
Cứ mỗi 04 chu kỳ điều trị: 03 chu kỳ đầu (mỗi chu kỳ “Trả 1, Tặng 1”); 01 chu kỳ tiếp theo miễn phí hoàn toàn. |
Cứ mỗi 04 chu kỳ điều trị: 03 chu kỳ đầu (mỗi chu kỳ “Trả 2, Tặng 2”); 01 chu kỳ tiếp theo miễn phí hoàn toàn. |
|
Mức 3 |
Kết quả đánh giá |
Cứ mỗi 04 chu kỳ điều trị: 02 chu kỳ đầu (mỗi chu kỳ “Trả 1, Tặng 1”); 02 chu kỳ tiếp theo miễn phí hoàn toàn. |
Cứ mỗi 04 chu kỳ điều trị: 02 chu kỳ đầu (mỗi chu kỳ “Trả 2, Tặng 2”); 02 chu kỳ tiếp theo miễn phí hoàn toàn. |
Quy định Đặc biệt cho Bệnh nhi (Dưới 18 tuổi)
Chương trình có chính sách nhân văn, ưu tiên tuyệt đối cho bệnh nhi :
- Bệnh nhi có chỉ định (U lympho Hodgkin kinh điển, PMBCL, Ung thư có MSI-H) sẽ KHÔNG CẦN đánh giá khả năng chi trả.
- Tất cả bệnh nhi đều được hưởng Mức hỗ trợ 3 hoặc tương đương Mức hỗ trợ 3.
- Chi tiết (Liều 2mg/kg/3 tuần):
- Cân nặng > 50kg: Áp dụng Mức 3 (Cứ 4 chu kỳ: 2 chu kỳ “Trả 1, Tặng 1”, 2 chu kỳ miễn phí hoàn toàn).
- Cân nặng < 50kg: (Dùng 1 lọ/chu kỳ) Cứ 8 chu kỳ: 4 chu kỳ đầu (cứ 1 chu kỳ tự trả, 1 chu kỳ miễn phí); 4 chu kỳ tiếp theo miễn phí hoàn toàn.
Quy định Hỗ trợ Dài hạn (Tất cả bệnh nhân)
Chương trình có quy định hỗ trợ đặc biệt cho các bệnh nhân đáp ứng tốt và điều trị lâu dài :
- Sau khi điều trị liên tục 24 chu kỳ (liều 200mg) hoặc 12 chu kỳ (liều 400mg), người bệnh sẽ nhận được 11 chu kỳ (liều 200mg) hoặc 06 chu kỳ (liều 400mg) MIỄN PHÍ HOÀN TOÀN tiếp theo, nếu vẫn còn chỉ định điều trị.
- Tổng liệu trình điều trị tối đa được hỗ trợ là 35 liệu trình (tương đương khoảng 2 năm).
Danh sách Bệnh viện Tham gia
Đây là thông tin mang tính hành động quan trọng nhất cho bệnh nhân, chỉ rõ nơi có thể tiếp cận chương trình.
Bảng 3: Danh sách 49 Bệnh viện trên Toàn quốc Tham gia Chương trình Hỗ trợ Keytruda (2024-2026)
|
Khu vực |
Tên Bệnh viện |
|
Miền Bắc |
Bệnh viện K (cả 3 cơ sở) |
|
Bệnh viện Bạch Mai |
|
|
Bệnh viện Phổi Trung ương |
|
|
Bệnh viện Ung bướu Hà Nội |
|
|
Bệnh viện Trung ương Quân đội 108 |
|
|
Bệnh viện Đại Học Y Hà Nội |
|
|
Bệnh viện Việt Đức |
|
|
Viện Huyết học và Truyền máu Trung ương |
|
|
Bệnh viện Hữu Nghị |
|
|
Bệnh viện Vinmec Times City |
|
|
Bệnh viện Đa khoa Tâm Anh Hà Nội |
|
|
Bệnh viện Đa khoa Thu Cúc |
|
|
Bệnh viện E |
|
|
Bệnh viện Bộ Công An 19-8 |
|
|
Bệnh viện Quân Y 103 |
|
|
Bệnh viện Tai Mũi Họng Trung ương |
|
|
Bệnh viện Ung bướu Hưng Việt |
|
|
Bệnh viện Hữu Nghị Lạc Việt (Vĩnh Phúc) |
|
|
Bệnh viện Đa khoa tỉnh Phú Thọ |
|
|
Bệnh viện Bãi Cháy (Quảng Ninh) |
|
|
Bệnh viện Đa khoa Quảng Ninh |
|
|
Bệnh viện Việt Tiệp Hải Phòng |
|
|
Bệnh viện Ung bướu Nghệ An |
|
|
Bệnh viện Ung bướu Thanh Hóa |
|
|
Bệnh viện Đại học Phenikaa |
|
|
Miền Trung |
Bệnh viện Trung ương Huế |
|
Bệnh viện Ung Bướu Đà Nẵng |
|
|
Bệnh viện Đà Nẵng |
|
|
Bệnh viện Đa khoa Hoàn Mỹ (Đà Nẵng) |
|
|
Bệnh viện Đa khoa Bình Định |
|
|
Bệnh viện Ung bướu Khánh Hòa |
|
|
Bệnh viện Đại học Y Dược Buôn Ma Thuột |
|
|
Miền Nam |
Bệnh viện Chợ Rẫy |
|
Bệnh viện Ung Bướu (TP.HCM) |
|
|
Bệnh viện Đại học Y Dược HCM |
|
|
Bệnh viện Quân Y 175 |
|
|
Bệnh viện Bình Dân |
|
|
Bệnh viện Thống Nhất |
|
|
Bệnh viện Nhân Dân 115 |
|
|
Bệnh viện Nhân Dân Gia Định |
|
|
Bệnh viện Truyền máu Huyết Học HCM |
|
|
Bệnh viện Đa khoa Thành phố Thủ Đức |
|
|
Bệnh viện Triều An |
|
|
Bệnh viện Vinmec Central Park |
|
|
Bệnh viện Đa khoa Tâm Anh TPHCM |
|
|
Bệnh viện Pháp Việt |
|
|
Bệnh viện Đại học Y Dược Shing Mark (Đồng Nai) |
|
|
Bệnh viện Ung bướu Cần Thơ |
|
|
Bệnh viện Ung bướu tỉnh Kiên Giang |
Phân tích Chuyên sâu và Kết luận
Báo cáo này cho thấy Pembrolizumab (Keytruda) đại diện cho một bước tiến khoa học vượt bậc trong điều trị ung thư, mang lại các đáp ứng bền bỉ và cải thiện tỷ lệ sống còn cho nhiều bệnh nhân mà trước đây được coi là không còn lựa chọn. Tuy nhiên, nó cũng mang đến hai thách thức song song và vô cùng lớn:
- Thách thức về An toàn: Quản lý các độc tính miễn dịch (irAEs) phức tạp, có khả năng đe dọa tính mạng, đòi hỏi chuyên môn y tế cao và sự theo dõi sát sao.
- Thách thức về Chi phí: Chi phí của liệu pháp miễn dịch là cực kỳ cao, tạo ra một rào cản tài chính gần như không thể vượt qua đối với phần lớn bệnh nhân.
Bối cảnh của Pembrolizumab tại Việt Nam cho thấy một nỗ lực có hệ thống và toàn diện để giải quyết đồng thời cả hai thách thức này.
Giải quyết Thách thức An toàn: Bằng cách cấp phép lưu hành chính thức và giới hạn việc thực hiện điều trị cũng như chương trình hỗ trợ trong 49 bệnh viện chuyên khoa ung bướu và bệnh viện đa khoa tuyến trung ương , hệ thống y tế Việt Nam đảm bảo rằng thuốc được quản lý bởi các đội ngũ bác sĩ và dược sĩ có đủ kinh nghiệm, cơ sở vật chất để chẩn đoán sớm và xử lý kịp thời các biến cố irAEs.
Giải quyết Thách thức Tiếp cận: Thay vì để gánh nặng tài chính cho bệnh nhân, một “hệ sinh thái” hỗ trợ đa bên (Bộ Y tế, MSD, Quỹ Ngày mai tươi sáng, EasyGop, Phytopharma) đã được thiết lập. Việc sử dụng một bên thứ ba độc lập (EasyGop) để đánh giá khả năng chi trả và phân bổ hỗ trợ theo mô hình “công bằng” (equity-based) – hỗ trợ nhiều hơn cho người khó khăn hơn – là một mô hình tiếp cận thuốc tiên tiến. Các chính sách đặc biệt, nhân văn như miễn đánh giá tài chính cho bệnh nhi 4 càng nhấn mạnh cam kết xã hội của chương trình.
Tóm lại, việc Pembrolizumab (Keytruda) được đăng ký và có một chương trình hỗ trợ bệnh nhân quy mô lớn, có cấu trúc rõ ràng tại Việt Nam cho thấy sự hội nhập nhanh chóng và trưởng thành của quốc gia vào các tiêu chuẩn điều trị ung thư tiên tiến nhất trên thế giới.
Đối với bệnh nhân và người nhà, điều quan trọng là phải hiểu rõ cả hai khía cạnh: (1) Lợi ích và rủi ro khoa học của thuốc, đặc biệt là nhận biết các dấu hiệu irAEs để báo cáo bác sĩ kịp thời; và (2) Các khía cạnh thực tiễn của chương trình hỗ trợ, chủ động liên hệ với các bệnh viện trong danh sách để được tư vấn về điều kiện tham gia và quy trình đánh giá tài chính.



